新年新气象新知识,今天要学习的是世界上已知的密度最小的气体—氢气!从它的制备到性质,包学习APP为同学们准备了一份终极“档案”。你值得拥有呦!

氢气的制备(拓展)
1
实验室制取氢气
(1)实验药品与反应原理
①药品:锌粒和 稀硫酸 (或 稀盐酸 )
②原理:Zn+H2SO4=ZnSO4+H2↑或Zn+2HCl=ZnCl2+H2↑
(2)反应装置
反应物的状态为固态和液态,反应条件为室温。发生装置和收集装置如下:
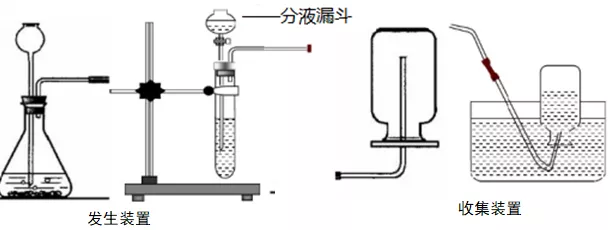
(3)实验现象
锌粒表面反应剧烈,生成大量气泡。

划重点!!!
(1)反应前一定要检查装置的气密性。
(2)氢气的密度比空气小,且不易溶于水也不与水反应,故可用向下排空气法或排水法收集。
(3)制取氢气时,长颈漏斗下端要伸入液面下,形成液封,防止气体逸出。
(3)发生装置中的长颈漏斗也可用分液漏斗替代,使用分液漏斗的优点是可控制反应的发生和停止,以及控制药品的滴加速率。
注意:使用稀盐酸与锌粒反应制取氢气,制取的氢气中可能混有挥发的HCl,收集过程中需要除杂。

2
工业制取氢气
目前工业制取氢气主要有几种方法:
①采用化石燃料制取氢气;
②从化工副产物中提取氢气;
③采用来自生物的甲醇、甲烷制取氢气;
④利用太阳能、风能等自然能量进行水的电解。

【示范例题】
例题1.(单选题) 收集氢气既可以用向下排空气法又可以用排水法,其原因是( )
A.比氧气轻,不跟水反应
B.氢气轻,微溶于水
C.比空气轻,相对分子质量比水小
D.比空气轻,难溶于水,不跟水反应
【答案】D
【解析】略
例题2.(单选题) 实验室制取氢气时,可选用的试剂是( )
A.氯酸钾和二氧化锰
B.空气
C.锌和稀硫酸
D.高锰酸钾
【答案】C
【解析】略
例题3.(填空题)请你根据如图回答有关问题:
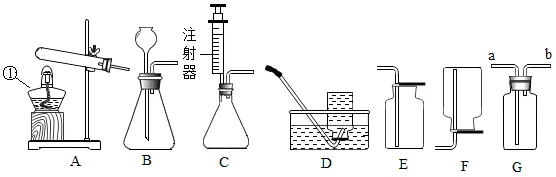
(1)写出仪器①的名称:( )
(2)实验室可用锌粒与稀硫酸反应制取氢气,可选用的发生装置为( ),若要用G装置收集氢气,气体应该从( )端进入。
【答案】(1)酒精灯
(2)B(或C);b
【解析】用锌粒与稀硫酸反应制取氢气,属于固液常温型,氢气密度比空气小,所以应从短管进气。
认识氢气的还原性(拓展)
1
实验装置

2
实验步骤
(1)检验氢气纯度;
(2)加热氧化铜,观察现象;
(3)停止加热,待装置冷却后停止通氢气。
3
实验现象
黑色的氧化铜变红。

4
实验结论
氢气具有还原性,发生的发应为H2+CuO=(△)Cu+H2O。
(1)氢气是可燃气体,燃烧前一定要先验纯,防止爆炸。
(2)加热氧化铜时,先均匀加热,再集中加热。
拓展:实验装置的改进

举手答
例题1.(填空题)反应停止后,若先撤掉氢气,则还原的金属铜可能( )。
【答案】被氧化
【解析】略
【示范例题】
例题1.(单选题) 下列说法不正确的是( )
A.H2在空气中燃烧的火焰为淡蓝色
B.利用H2的还原性可以冶炼金属
C.氢气是一种新能源
D.收集满氢气的集气瓶正放在桌子上
【答案】D
【解析】氢气的密度比空气小,收集满氢气的集气瓶应倒放在桌子上。
例题2.(单选题) 经验纯H2还原氧化铜时,应先通氢气后加热,原因是
()
A.防止铜被氧化
B.防止氢气被氧化
C.防止混合气体发生爆炸
D.防止氢气逸出
【答案】C
【解析】先通氢气后加热,防止混合气体发生爆炸。



